DSE Chem 微觀世界 II 攻略|HKEAA 要求+鍵結 VSEPR+氫鍵陷阱+真題
Topic VI 微觀世界 II 深入 bonding 四類、VSEPR 六形狀、van der Waals vs 氫鍵。本篇整理必背 flashcard、高頻失分陷阱(氫鍵條件/bond angle/物性預測)、Level 5 答題 framework 同兩題 structured walkthrough。
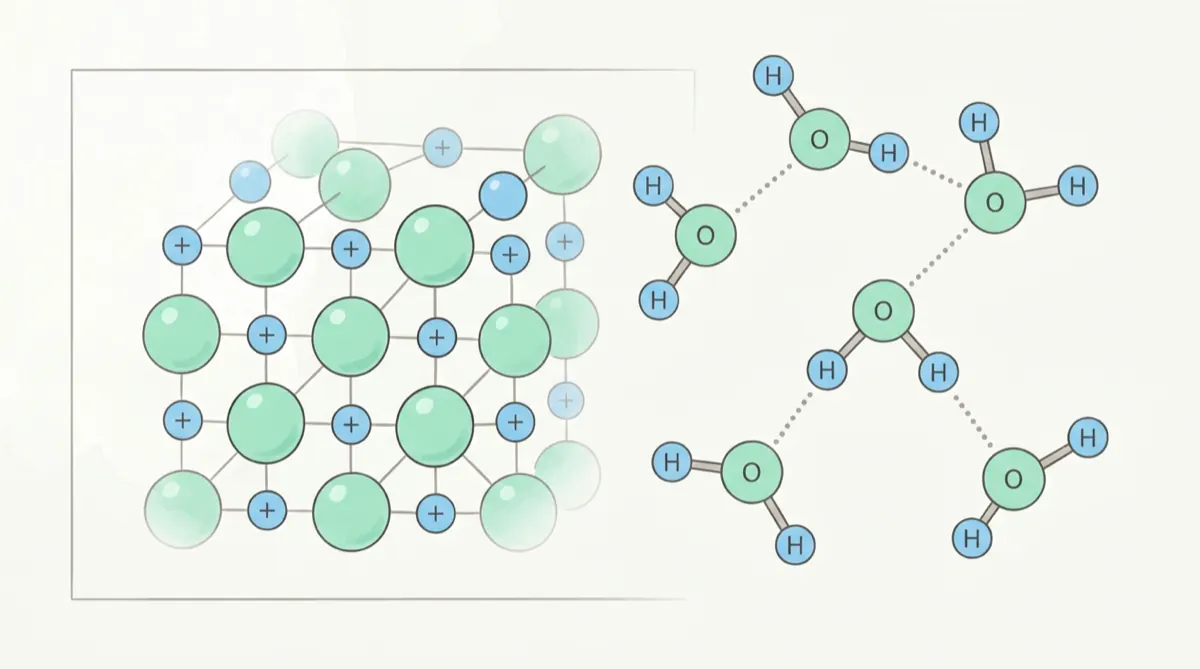
呢個 topic 俾好多同學一個錯覺:「咪即係 F.3 學過嘅 ionic vs covalent 囉」。其實 HKEAA 將 Microscopic World II 拎出嚟做必修 Topic VI,目的就係要你由「記鍵結名」跳去「解釋物性、預測形狀、比較分子間作用力」。2019 至 2024 每一屆 Paper 1B 都有題目圍繞呢三件事。
最痛嘅係呢個 topic 嘅 concept 互相勾連:答 boiling point 要用 intermolecular force,答 intermolecular force 要認 VSEPR 形狀先判斷到 polarity,答 polarity 又要識畫 Lewis + 電負性差。連鎖反應下,只要一步錯,後面五分全部走數。我哋就逐層拆開佢。
HKEAA 呢 topic 要求:五個 sub-section 點分
官方指引將 Topic VI 分五段:電負性與極性、分子形狀、晶體結構四類、分子間作用力、溶解性預測。考評局要求嘅能力係「由結構推物性」,唔係抄課本 definition。
指引要求學生「運用 VSEPR 模型預測簡單分子的形狀」、「比較 ionic、giant covalent、simple molecular 及 metallic 晶體的物理性質並以結構解釋」、「辨認氫鍵形成條件並解釋其對沸點、溶解度的影響」。重點落在「結構 → 性質」嘅 causal link。
| 題型 | 常見問法 | 2019–2024 出現頻率 |
|---|---|---|
| MC | VSEPR 形狀、晶體物性、極性判斷 | 每年 3–5 題 |
| Structured | 氫鍵解釋沸點異常、Group 14/16 趨勢 | 2019/2021/2023 |
| Explain | 為何 CO₂ 非極性而 H₂O 極性、diamond vs graphite 導電 | 每年 1 題 |
必背 flashcard · 7 張核心
① VSEPR 六種形狀 + 鍵角
記憶鉤:lone pair 多一對 → bond angle 細一啲。
② 四類晶體物性對比
③ 氫鍵形成三條件
陷阱:HCl、H₂S、PH₃ 冇氫鍵 — Cl / S / P 電負性唔夠大。
④ van der Waals 力三因素
⑤ 極性分子判斷三步
⑥ 同素異形體三對
⑦ Like dissolves like 溶解規則
⑧ 同素異形體完整對比
Oxygen:O₂(順磁性, 生物需要)vs O₃ ozone(bent, 吸 UV, 平流層保護)。Sulfur:S₈ crown 環(rhombic 室溫穩定 vs monoclinic 高溫形態);加熱至 >160°C 出現 plastic sulfur(長鏈)。
考點:「同一元素 different allotropes 物性大異」原因 = 鍵結 / 晶體結構唔同,非分子式差異。
⑨ Trigonal bipyramidal + lone pair 位置
6 對:octahedral (SF₆) 90° 全部一樣,lone pair 出現 → square pyramidal(BrF₅)→ square planar(XeF₄)。DSE 通常只要求識認 PCl₅ 同 SF₆;但 seesaw 偶爾出 distractor MC。
高頻陷阱 · 4 個最典型失分位
陷阱 1:講 HCl 之間有氫鍵
好多考生見到 H 同電負性 atom 鍵合就寫「氫鍵」。但 Cl 電負性 3.0 而原子半徑大、電荷密度低,δ+ 嘅 H 吸唔到 Cl 嘅孤電子對。HCl 分子間只有 dipole-dipole + vdW,冇氫鍵。真正具備氫鍵條件只限 F / O / N 三個。
真題:2020 DSE Chem Paper 1B Q2(b) 比較 HF 同 HCl 沸點,評卷員報告指出半數考生錯寫「HCl 也有氫鍵只係較弱」。
陷阱 2:VSEPR 漏 lone pair 影響
寫 NH₃ 係「三角平面」、H₂O 係「直線」—— 冇考慮到 N 有 1 對 lone pair、O 有 2 對 lone pair。Lone pair 嘅排斥力大過 bond pair,會壓細 bond angle。正確:NH₃ pyramidal 107°、H₂O bent 104.5°。
記憶:數「electron pairs 總數」先定幾何,然後「bond pairs」先定形狀名稱。
陷阱 3:boiling point trend 解釋唔齊
答 Group 17 沸點遞增,要寫:「分子電子數/大小增加 → 瞬時偶極引致嘅 van der Waals 力增強 → 需要更多能量克服 → b.p. 上升」。只寫「vdW 增加」得 1/2 分;冇寫「電子數」或「needs more energy to overcome」攞唔到第二分。
真題:2022 Paper 1B Q4(a) 要求解釋 HF > HI > HBr > HCl 嘅沸點次序,評卷員點名要「氫鍵 vs vdW 兩種力分開討論」。
陷阱 4:giant vs simple molecular 物性撈亂
SiO₂(giant covalent)m.p. ≈ 1710°C;CO₂(simple molecular)−78°C 就昇華。兩者同屬碳族氧化物但物性相差成千度。寫「SiO₂ 係 simple molecular」直接 0 分 — SiO₂ 係 3D 共價網,每個 Si 同 4 個 O 相連。
判斷準則:睇到「金剛石結構/層狀/3D 網」= giant;睇到細分子式(CO₂、I₂、C₆₀)= simple molecular。
陷阱 5:氫鍵寫「氫原子同氟/氧/氮間嘅吸引力」太淺
HKEAA 完整定義:「氫鍵係一種分子間吸引力,其中 δ+ 嘅 H 原子(鍵合於 highly electronegative 嘅 F/O/N)吸引另一個分子上 F/O/N 嘅 lone pair」。三個條件:(1) H 必須直接 bond 去 F/O/N;(2) 接受方必須係 F/O/N 帶 lone pair;(3) 空間夠接近方向性要對。
單寫「H 同 F/O/N 之間嘅吸引力」只得 1/2 分,冇 lone pair + electronegativity 字眼扣埋第 2 分。
陷阱 6:Diamond vs Graphite 導電解釋唔具體
Diamond:每個 C sp³ 用晒 4 個 valence electron 做 σ bond,無 free / delocalised electron,所以唔導電。Graphite:每個 C sp², 用 3 個做 σ,剩 1 個 p 電子形成 delocalised π-electron cloud between layers,電子可沿 layer 移動 → 導電(沿平面);垂直方向唔導電因為 layers 只靠 vdW。
答題必有 keyword「delocalised electron / free electron parallel to layers」。
答題 framework · 結構推物性三層
呢個 topic 嘅 structured 題大多要求「解釋物性差異」。Level 5 答案永遠有三層:identify bonding → state force involved → link to property。
| 層次 | Level 4(一般) | Level 5(拎滿分) |
|---|---|---|
| 結構識別 | 「簡單分子」 | 「simple molecular crystal;分子由共價鍵連住、分子之間只有 vdW」 |
| 作用力 | 「弱的分子間力」 | 「weak van der Waals forces only, no hydrogen bonding as no H-F/O/N」 |
| 物性推演 | 「m.p. 低」 | 「little energy needed to overcome intermolecular forces → low m.p.」 |
真題 walkthrough · 2 題
真題 1:2021 Paper 1B · 冰浮於水面 · 3 marks
題目(paraphrase):用分子間作用力解釋點解冰嘅密度比液態水低。
Model:In ice, each water molecule forms four hydrogen bonds with neighbouring molecules, locking them in a rigid tetrahedral lattice with open cavities (1). This arrangement keeps molecules at fixed, relatively large separations (1). When ice melts, some hydrogen bonds break and molecules pack more closely together, so liquid water has higher density than ice (1).
Hydrogen bond = "attractive force between δ+ H (bonded to F/O/N) of one molecule and lone pair of F/O/N in another molecule";Giant covalent = "3-D network of atoms joined by strong covalent bonds throughout the crystal";Van der Waals = "weak attraction between temporary / induced dipoles of neighbouring molecules";Metallic bond = "electrostatic attraction between positive metal ions and delocalised valence electrons / sea of electrons"。2023 考評員報告點名:寫 vdW 冇「temporary / induced dipole」;寫金屬鍵冇「delocalised / sea」扣 ½ mark。
真題 2:2023 Paper 1B · CO₂ 非極性 · 2 marks
題目(paraphrase):儘管 C=O 有明顯鍵極性,解釋點解 CO₂ 係非極性分子。
Model:C atom has 2 bonding regions and no lone pair, so by VSEPR the molecule is linear with bond angle 180° (1). The two C=O dipole moments are equal in magnitude but opposite in direction, cancelling exactly, so the net molecular dipole is zero — CO₂ is non-polar (1).
學習路徑 · 3 步打通
去 /dse-chem/microscopic-world-ii/ 睇齊五個 sub-section scoring points。
下載 DSE 神器 Chem App,篩 Topic VI 鍛鍊形狀/物性題感。
去 Flashcard 區,spaced repetition 覆盤 VSEPR 六形狀 + 氫鍵條件。
延伸閱讀
電子轉移 concept 建基喺鍵結能力上。
Bond enthalpy 會用到呢一 topic 嘅鍵結知識。
2,000+ 題覆蓋全 15 topic。
承 微觀世界 I 嘅原子結構,covalent + IMF 概念接 碳化學 嘅分子形狀同 化學物料 嘅聚合物設計;全科網絡見 HKEAA 分析。