DSE Chem 氧化還原+電池+電解攻略|HKEAA+SRP 表+陷阱+真題
Topic VII 氧化還原、化學電池同電解係 Paper 1B 分數大戶。本篇整理氧化數八條規則、半方程式配平步驟、SRP 表應用、galvanic/electrolytic cell 對比、5 個高頻陷阱同真題 walkthrough。
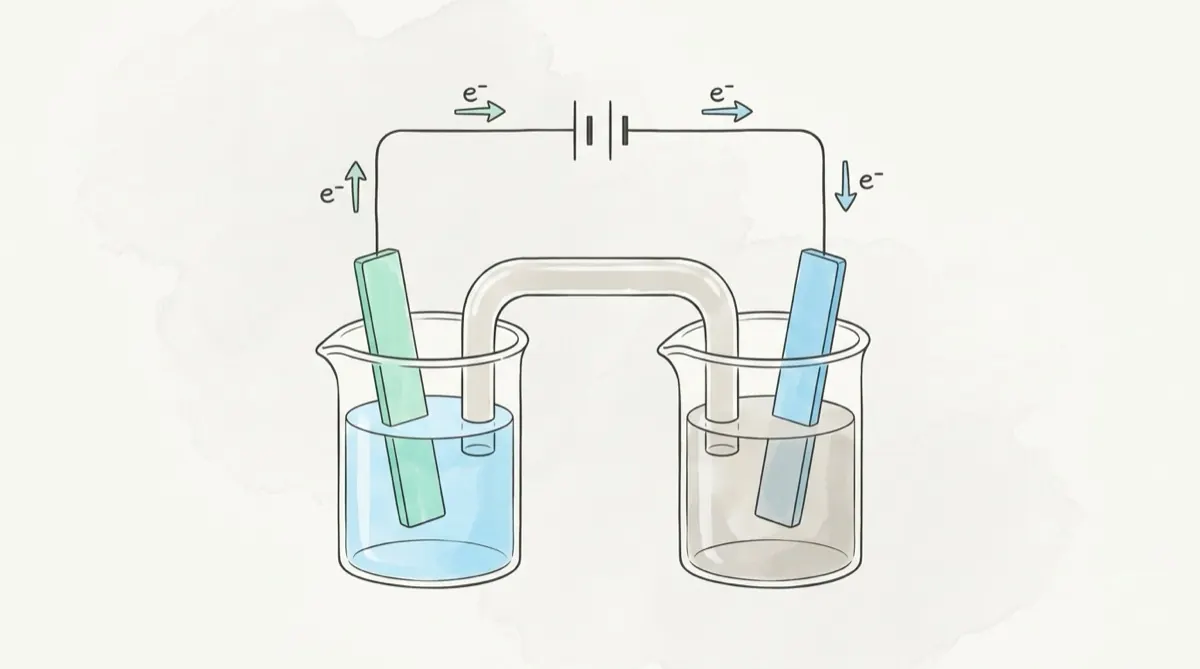
如果有人問 DSE Chem 邊個 topic 佔 Paper 1B 分數最多,答案十次有九次係 Topic VII — 氧化還原、化學電池同電解。由 2019 到 2024 每屆 Paper 1B,氧化還原佔最少 12 分,有幾年更加超過 18 分。原因好簡單:呢個 topic 可以同酸鹼、過渡金屬、有機反應 crossover,所以考評局好鍾意出。
偏偏同學最易失分嘅都係呢度。氧化數寫錯、半方程式配平搞亂 H⁺/H₂O/e⁻ 順序、galvanic vs electrolytic cell 兩個 cell 搞錯 anode/cathode 極性 — 每一個都係 −1 到 −3 分嘅傷。呢篇拆清氧化數八條規則、半方程式三步配平、SRP 表應用同兩個 cell 嘅 polarity convention。
HKEAA 呢 topic 要求:三大主線
官方指引將 Topic VII 拆三層:氧化還原本身(概念 + 氧化數 + 配平)、化學電池(galvanic cell + SRP + EMF)、電解(電極反應 + Faraday)。三層都要會由 half-equation 推 overall equation,再推 observation。
指引要求學生「利用氧化數變化辨認氧化還原反應及氧化/還原劑」、「配平氧化還原反應方程式」、「應用標準還原電位預測化學電池嘅可行性」、「解釋電解過程中嘅電極反應(包括水溶液及熔融狀態)」。強調嘅係 quantitative prediction + mechanism 兩層。
| 題型 | 常見問法 | 2019–2024 出現頻率 |
|---|---|---|
| MC | 氧化數判斷、SRP 預測、電解產物 | 每年 5–7 題 |
| Structured | KMnO₄ 滴定、Cu-Zn cell、鹽水電解 | 每年 1–2 題 |
| Calculation | Faraday Q=It、mole 電子轉換 | 2019/2021/2024 |
必背 flashcard · 7 張核心
① 氧化數八條規則
② 半方程式三步配平
③ 常見 10 對 SRP pair
用途:E°右上氧化 E°左下。
④ Galvanic vs electrolytic cell 對比
記憶:兩者 anode 永遠都係 oxidation 發生處,只係極性牌相反。
⑤ 電鍍三步驟
⑥ 電解鹽水(brine)產物
⑦ Faraday 公式 Q = It + n = Q / (zF)
高頻陷阱 · 5 個最典型
陷阱 1:單質氧化數寫錯
寫 O₂ 中 O 嘅氧化數係 −2。錯!Element 本身處於未結合態(不論單原子或雙原子),氧化數一律等於 0。所以 O₂ 中 O = 0、Cl₂ 中 Cl = 0、Na(s) 中 Na = 0。呢條係規則第一條,但亦係最多人忘記嘅一條。
陷阱 2:Electroplating anode/cathode 寫反
想鍍銀喺匙羹上,寫「匙羹接 anode」。錯!Anode 係 oxidation 發生處會溶解金屬;如果匙羹接 anode,匙羹本身會被氧化溶走。正確:被鍍物件永遠接 cathode;鍍料金屬接 anode 作溶出源。
真題:2022 Paper 1B Q8 要考生描述電鍍 gold 過程,評卷員報告指 25% 考生將 anode/cathode 對調。
陷阱 3:Aqueous electrolysis 漏水放電
電解稀 NaCl(aq) 寫 cathode 產物係 Na。錯!水溶液電解時要比較離子同水嘅 E°。Na⁺ (−2.71) 遠負過 H₂O (−0.83),所以 cathode 實際 discharge 嘅係水:2H₂O + 2e⁻ → H₂ + 2OH⁻。Na⁺ 留喺溶液中。
陷阱 4:Cu-Zn cell EMF 計錯 sign
Cu²⁺/Cu = +0.34 V;Zn²⁺/Zn = −0.76 V。正極(cathode)係 E° 較高嗰個 → Cu²⁺/Cu。EMF = (+0.34) − (−0.76) = +1.10 V。好多考生寫 E°(anode) − E°(cathode) 俾成 −1.10,直接扣分;記住用大減細,而且條 convention 永遠 cathode − anode。
陷阱 5:Q=It 時間未換秒
題目「通電 30 分鐘」要換 1800 s;題目「半小時」要 1800 s;不足分鐘就乘 60。單位錯一次,所有 downstream 數字全部離譜。
陷阱 6:Half-equation 漏 state symbol / 電子唔平衡
寫「Zn → Zn²⁺ + 2e」— state 漏、電子符號 e⁻ 寫成 e、前面 stoichiometric coefficient 唔標明都算 half-scored。Full mark 寫法:Zn(s) → Zn²⁺(aq) + 2e⁻,三個 state + 電子明確標 minus sign。2023 Paper 1B Q5 考評員報告指出,約 42% 考生寫 half-equation 時漏 state symbol,單單呢點就損失 1–2 mark。
口訣 · OIL RIG + AN OX / RED CAT
氧化還原三個最易混淆嘅一對對概念,用英文短 mnemonic 最快記熟。背熟之後寫 half-equation 同標極性都唔會撈亂。
Oxidation Is Loss (of electrons)
Reduction Is Gain (of electrons)
即係 Zn → Zn²⁺ + 2e⁻ 係 oxidation(失電子);Cu²⁺ + 2e⁻ → Cu 係 reduction(得電子)。
ANode = OXidation occurs here
REDuction = at CAThode
兩個 cell(galvanic / electrolytic)anode 永遠都係 oxidation,只係極性正負牌相反。Galvanic anode = 負極;electrolytic anode = 正極。
Level 5 scoring keyword bank
以下 keyword 考評局報告反覆提及 — 答 explanation 題時每一個都值 ½ 至 1 mark。
| 情境 | Level 5 wording |
|---|---|
| Oxidising agent | a species that gains electrons / undergoes reduction / causes oxidation of another species |
| Electrolyte | a substance which conducts electricity in molten or aqueous state and undergoes chemical decomposition |
| Salt bridge role | completes the circuit / allows ion flow to maintain electrical neutrality in both half-cells |
| Why Cl⁻ discharged over OH⁻ (concentrated brine) | due to the higher concentration of Cl⁻ (overriding E° prediction); mention overpotential for Level 5* |
| Self-indicator (KMnO₄) | KMnO₄ is purple; when reduced to Mn²⁺ it becomes almost colourless. End-point = first permanent pale pink tinge |
2024 Paper 1B 考評員報告指出,Redox 相關題目之中「electrolysis of concentrated NaCl(aq)」嘅 anode 解釋係高分題關鍵:考生要同時指出 (1) Cl⁻ 比 OH⁻ 被選擇性放電;(2) 原因係 Cl⁻ 濃度較高 + overpotential 降低氧氣放電傾向。只寫一個原因通常只得 1/2 mark。
答題 framework · 電池 / 電解題四步
| 步驟 | Level 4 | Level 5 |
|---|---|---|
| ① 極性標記 | 「Zn 係 anode」 | 「Zn anode (−ve, oxidation); Cu cathode (+ve, reduction)」 |
| ② 半方程 | 「Zn → Zn²⁺」 | 「Zn(s) → Zn²⁺(aq) + 2e⁻」(state + electron 齊) |
| ③ 觀察 | 「Zn 溶解」 | 「Zn rod dissolves, becomes thinner; blue Cu²⁺ fades as Cu deposits on Cu electrode」 |
| ④ 鹽橋作用 | 漏 | 「salt bridge completes circuit, allows ion flow to maintain charge balance」 |
真題 walkthrough · 2 題
真題 1:2020 Paper 1B · KMnO₄ 滴定 Fe²⁺ · 3 marks
題目(paraphrase):描述酸化 KMnO₄ 滴定 Fe²⁺(aq) 嘅顏色變化同終點判斷。
Model:MnO₄⁻ + 8H⁺ + 5Fe²⁺ → Mn²⁺ + 4H₂O + 5Fe³⁺ (1). During titration, purple KMnO₄ is decolourised as it reacts with Fe²⁺, solution remains nearly colourless (1). End-point reached when one extra drop gives a permanent pale pink tinge, indicating all Fe²⁺ consumed — KMnO₄ acts as self-indicator (1).
真題 2:2023 Paper 1B · 電解稀 H₂SO₄ · 4 marks
題目(paraphrase):以 Pt 電極電解稀 H₂SO₄(aq),寫出兩極半方程式,描述產物及體積比。
Model:Cathode (−): 2H⁺(aq) + 2e⁻ → H₂(g) (1). Anode (+): 2H₂O(l) → O₂(g) + 4H⁺ + 4e⁻ (1) — SO₄²⁻ is not discharged because S is already at highest oxidation state. Mole ratio H₂:O₂ = 2:1 (1), so gas volume ratio at same T/p = 2:1 (1). Net: electrolysis of water.
學習路徑 · 3 步
去 /dse-chem/redox/ 記熟 DSE 常考 10 對 pair。
下載 DSE 神器 Chem App,做 30 題半方程式 + 20 題 Faraday。
去 Flashcard 區,做成自己嘅 polarity 記憶表。
延伸閱讀
Cell EMF 實係 ΔG 嘅 redox 版。
氧化還原亦可達平衡(Fe³⁺/SCN⁻)。
2,000+ 題覆蓋全 15 topic。
Redox 係 金屬 活性序同 工業化學(電解鋁、電鍍、燃料電池)嘅核心 mechanism;滴定類 redox 題亦見於 分析化學。評核重點見 HKEAA 分析。